FCN-159片在成人NF1相关PN的1/2期研究已完成入组,正在随访中,共入组82例患者,包括1期19例、2期63例。
本次为III期临床研究,该项临床研究已得国家食品药品监督管理局药品评审中心的批准,临床试验登记号为CTR20231840。本项研究开展15个临床研究中心,预计在全国范围内招募162例神经纤维瘤1型患者。
招募主要入选标准
18岁以上,必须为NF1丛状肿瘤患者,并符合NF诊断标准中的任意两项。
A:对于无父母患病史者,满足以下≥2条临床特征可被诊断为NF1:
6个或以上咖啡牛奶斑(café-au-lait macules,CALMs):在青春期前直径>5 mm
或在青春期后直径>15mma
腋窝或腹股沟区雀斑a
2个或以上任何类型的神经纤维瘤或1个pNF视神经胶质瘤(Optic pathway glioma,OPG)
裂隙灯检查到2个或以上Lisch结节,或光学相干层析成像(OCT)/近红外(NIR)影像检查到2个或以上的脉络膜异常
特征性骨病变,如蝶骨发育不良b、胫骨前外侧弯曲,或长骨假关节生成在正常组织(如白细胞)中具有等位基因变体分数达50%的致病杂合子NF1变异体
B:对于有父母患病史者,满足以上≥1条临床特征可被诊断为NF1。
已开展的临床中心
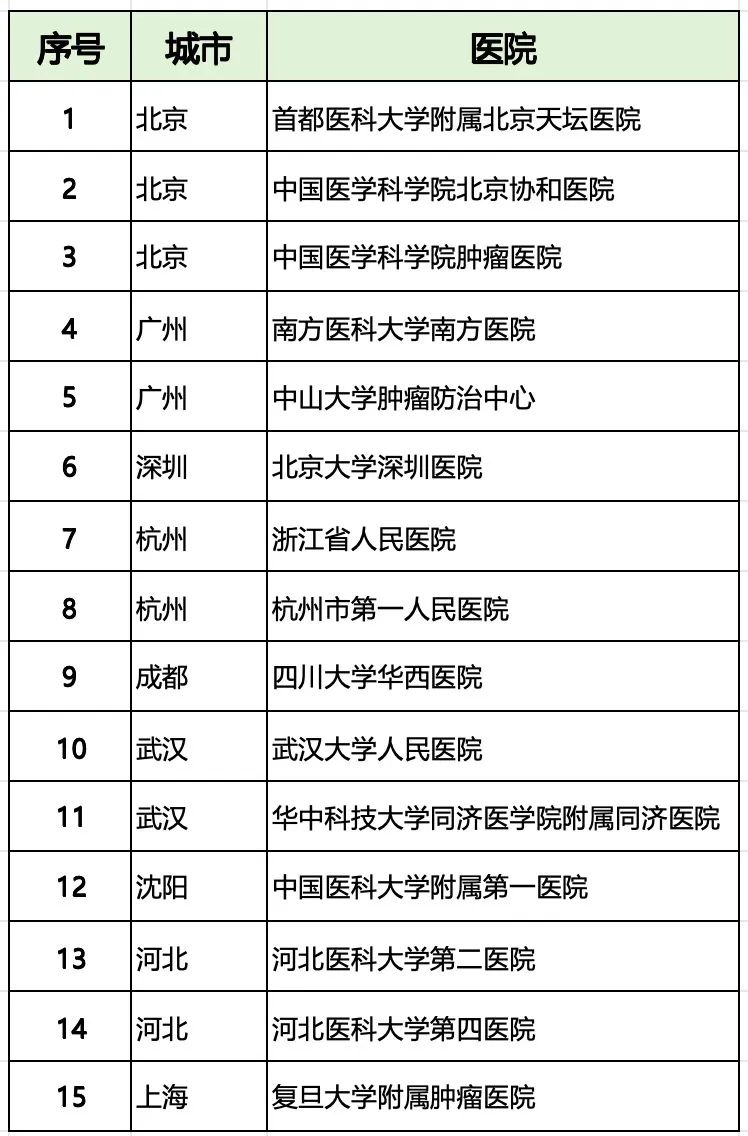
参与本次临床试验您将获得
经研究医生判断,如果您符合本研究的入选条件并自愿参加,您将获得:
1、本次临床试验的药物由申办方提供;
2、适当的交通、营养补助;
3、专业研究医生的病情指导。
研究期间,将密切监测您的健康及安全,我们的筛选流程旨在确保您适合参加本研究。
如果您对此项研究感兴趣,可扫描下方二维码填写表单登记。登记后,我们将与您联系。

您也可以通过以下联系方式与研究团队取得联系。
联系人:罗女士
联系邮箱:Adela.luo@cord.org.cn
联系微信:CORD17(添加时,请注明神经纤维瘤(NF)患者)
| 神经纤维瘤(NF)
神经纤维瘤病(Neurofibromatosis,简称NF),又称多发性神经纤维瘤,是一种常染色体显性遗传性疾病,是由神经膜细胞和其他支撑周围神经纤维的细胞组成,累及神经、肌肉、骨骼、内脏、皮肤等全身各个系统,属于多系统疾病。神经纤维瘤病分为三种:神经纤维瘤病1型(NF1),患病率为1/3000,神经纤维瘤病2型(NF2),患病率1/60000, 以及神经鞘瘤病。虽然这是一种罕见病,但它不分种族。然而,国内外对于NF的科学普及程度较低,导致患者不能及早发现并得到治疗,甚至被误诊和延误治疗,给患者和家庭带来沉重的负担。
丛状神经纤维瘤(PN)是NF1的主要表现之一,存在PN表现的NF1患者约为20%-50%。PN可沿神经轴索弥漫性生长,呈浸润性,累及多条神经干及其分支,破坏深层的肌肉组织,骨骼组织甚至内脏器官,导致外观和骨骼畸形,并因神经受损,会伴有严重的疼痛、感觉异常。体积的缩小可改善疼痛、外观及功能障碍,因此缩小肿瘤是NF1治疗的主要目标。