导语
2025年7月12-13日,蔻德罕见病中心与瑞鸥公益基金会在杭州联合主办患者社群推动药物研发赋能会暨全国罕见病患者组织网络年会。
会议以 “患者社群推动自救式药物研发” 为核心,形式与内容有新突破。围绕药物研发全流程设四大主题分享,邀多领域专家参与,通过四个工作坊促进患者与专家深度交流,旨在解决各阶段核心问题,沉淀经验、形成共识、助力行动。
此次赋能会吸引66个疾病的120位代表,含39个患者组织代表。会上特设 “微光博物馆”,参会者的信物成为情感桥梁与对话媒介,传递个体故事的温度与力量。
蔻德罕见病中心将通过连载发布本次赋能会的相关内容,本篇为系列内容15

李龙承《生命的“信息修改器”——小核酸药物如何精准狙击罕见病》
中美瑞康创始人李龙承博士分享的主题是《生命的“信息修改器”——小核酸药物如何精准狙击罕见病》。
小核酸药物作为第三次制药革命的核心力量,正以 “信息编辑” 的精准逻辑,破解传统疗法难以触及的基因难题。
一小核酸药物:多元化的 “基因工具箱”
小核酸药物通过靶向基因表达上游的 RNA,实现对遗传信息的精准调控,形成了多元化的技术体系:
单链反义寡核苷酸(ASO) 分为两类:Gapmer 通过 DNA 片段激活 RNase H 酶降解靶 RNA,实现基因敲低;位点阻断型则通过结合 RNA 调控剪接(如外显子跳跃 / 包含),增加功能蛋白表达。治疗脊髓性肌萎缩症(SMA)的诺西那生、杜氏肌营养不良症(DMD)的 4 款药物均基于此机制。
双链 RNA 包括小干扰 RNA(siRNA)、小激活 RNA(saRNA)等。siRNA 通过 RNA 干扰机制降解异常 mRNA,适用于毒性蛋白蓄积疾病;saRNA 则能激活内源性基因表达,弥补功能缺陷,是中美瑞康的核心技术方向。
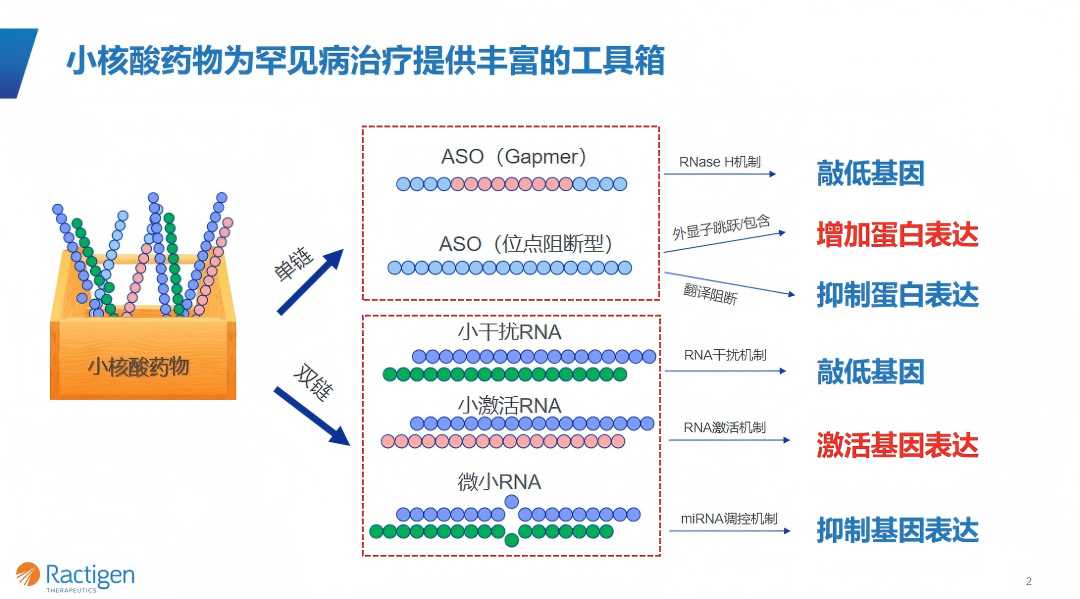
与小分子、抗体药相比,小核酸药物具有三大突破:理论上可靶向任意基因(突破传统 “不可成药” 限制);基于碱基互补原则实现理性设计,开发周期缩短至传统药物的 1/3;临床阶段成功率是小分子药的 10 倍以上,且生产工艺简单、成本可控。
二个性化治疗:从 “奇迹案例” 到体系化实践
2018 年,波士顿儿童医院为 CLN7 巴顿病患者 Mila 定制的 ASO 药物 Milasen,仅用 10 个月完成从设计到给药,使癫痫发作减少 70%,开启了 “N-of-1”(单患者定制)治疗时代。这一案例推动 FDA 出台系列指南,规范个性化小核酸药物研发。
非营利组织 n-Lorem 基金会成为标杆,为全球患者数≤30 人的超罕见病提供免费 ASO 治疗。截至 2025 年,该机构接收 350 份申请,180 项进入开发,30 余例完成 IND 申报并给药,单例成本约 130 万美元,从设计到用药周期仅 15-18 个月。
其核心逻辑在于平台化效率:利用患者 iPS 细胞和类器官验证药效,简化动物实验;标准化生产流程压缩周期,使超罕见病患者摆脱 “无药可医” 的绝境。

三国内可行性:技术成熟与待解难题
国内小核酸药物研发已具备技术基础:药明康德、凯莱英等企业可完成从设计到生产的全流程;研究者发起的临床试验(IIT)机制为罕见病开辟快速通道;iPS 细胞和类器官技术可替代动物模型验证药效。
但核心挑战仍存:精准诊断是前提 —— 需明确基因突变与疾病的因果关系(如渐冻症多基因突变的主次区分);发起方与资金链待明确 —— 药企因盈利属性难以主导,需患者组织、非营利机构牵头;成本控制需突破 —— 国内单例开发成本约 300-500 万元,仍需公益基金、医保政策支持。
四中美瑞康的实践:从机制创新到临床突破

中美瑞康聚焦 saRNA 技术,推动两款核心药物进入临床:
RAG-18(治疗 DMD/BMD)
DMD 因抗肌萎缩蛋白基因缺陷导致肌肉持续损伤,传统疗法仅能覆盖 10% 患者。RAG-18 通过 saRNA 激活内源性 Utrophin 蛋白(功能类似抗肌萎缩蛋白),实现 100% 患者覆盖。临床前数据显示,其可显著上调骨骼肌和心肌中 Utrophin 表达,减轻肌肉损伤,改善运动功能。该药物获 FDA “儿科罕见病” 和 “孤儿药” 双认证,预计 2025 年第四季度提交美国 IND 申请。
RAG-17(治疗 ALS)
针对 SOD1 基因突变导致的肌萎缩侧索硬化症(ALS),RAG-17 通过 siRNA 敲低有毒蛋白。IIT 研究显示,其疗效优于已上市的 Tofersen:患者功能评分下降速率减缓 60%,肺功能改善,生物标志物 NfL 水平降低 56%。2025 年美国神经病学学会(AAN)年会上,该成果获 “杰出摘要” 奖,目前 I 期临床进展顺利。
从 “技术突破” 到 “普惠可及”
小核酸药物正将罕见病治疗从 “碰运气” 的试错模式,推向 “按图索骥” 的精准时代。随着 n-Lorem 等模式的成熟、国内技术链条的完善,以及患者组织的积极推动,“一款药物救一个患者” 的奇迹,有望成为更多罕见病家庭的希望。正如李龙承所言:“小核酸的价值,在于让每个基因突变都有被修正的可能。”
蔻德罕见病中心&瑞鸥公益基金会将持续关注和参与推动罕见病患者社群推动药物研发这一议题的工作。如您对这一议题有兴趣,希望参与交流、进行项目合作、提供其他支持等,都可以与我们取得联系,请您留下基础信息,我们会及时与您取得联系,共同为罕见病患者社群早日实现有药可医而努力!
