昨天,拜耳发布了2025年财报。
财报中披露,公司已正式终止庞贝病基因疗法 ACTUS-101 的临床研究,转而将资源集中于另一款同类候选药物。
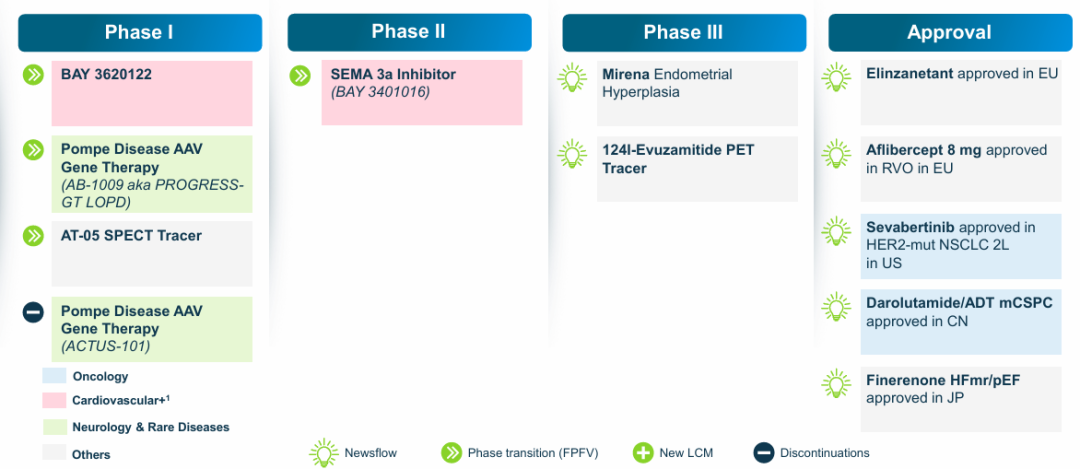
该疗法一期临床试验进展不及预期,仅入组 7 名患者。拜耳表示,将把研发资源全面转向二代候选药物 AB-1009。目前,AB-1009 已获得美国 FDA 授予的快速通道资格,并正式启动 I/II 期临床试验。
拜耳在 2020 年以20亿美元预付款收购AskBio时,同步获得两款针对晚发型庞贝病的 AAV 基因疗法,ACTUS-101 便是其中之一,且该疗法在收购完成时已进入临床阶段。基于研发效率与临床潜力的综合评估,拜耳最终做出止损、聚焦优势管线的决策。
与已终止的 ACTUS-101 相比,二代庞贝病 AAV 基因疗法 AB-1009 在研发设计与监管进展上均具备明显优势。该疗法已获得美国 FDA 快速通道和孤儿药双重资格认定,并于 2026 年初在美国启动 1/2 期临床试验,旨在从根源上解决庞贝病的遗传缺陷。
加州大学尔湾分校健康 ALS 及神经肌肉中心主任、AB-1009 项目首席研究员 Tahseen Mozaffar 博士表示,这款在研基因疗法致力于修复患者的基因突变,探索提升体内酸性 -α- 葡糖苷酶的生成水平,从而减少患者对外源性酶替代疗法的依赖。
一代疗法 ACTUS-101 以肝脏为靶向,而 AB-1009 采用 AAV8 载体直接靶向肌肉组织 —— 这正是庞贝病患者发生进行性肌肉变性的核心病灶。同时,其搭载的 GAA 基因经过密码子优化,并搭配组织特异性启动子,可显著提升酶在肌肉组织中的表达效率。
值得关注的是,中国生物技术公司信念医药在这一研发进程中发挥了关键作用。信念医药此前向 AskBio 授予了 AAV 衣壳的特许使用权,并提供关键的 AAV 载体生产服务。在双方合作开发框架下,信念医药与 AskBio 紧密协作,有力推动了 AB-1009 新药临床试验申请(IND)的成功获批。