3月16日,舶望制药有限责任公司(简称“舶望制药”)是一家临床阶段生物科技公司,宣布其在研siRNA疗法BW-20805获得美国食品药品监督管理局(FDA)授予快速通道资格(Fast Track Designation,FTD),用于治疗遗传性血管性水肿(hereditary angioedema,HAE)。
BW-20805是一种靶向前激肽释放酶 (prekallikrein,PKK)的siRNA疗法,通过靶向PKK mRNA而抑制PKK的表达,有望为HAE患者提供长效的发作预防。PKK是目前HAE治疗领域已获得充分验证的作用靶点。舶望制药目前在成人HAE患者中开展II 期临床研究,预计将于2026年下半年完成II 期临床试验,并随后启动III期临床研究。
舶望制药联合创始人兼首席执行官舒东旭博士表示:“快速通道资格的授予,反映了HAE患者群体存在显著的未满足医疗需求,也肯定了BW-20805作为一种全新治疗方案的潜力。我们已经积累了可观的临床数据,充分证实了BW-20805的潜力。近期我们在美国过敏、哮喘与免疫学会年会(AAAAI)上公布的数据显示,BW-20805可显著降低血浆PKK水平,并实现具有临床意义的HAE发作率降幅。我们期待加快推进BW-20805的临床开发,力争为患者带来一种可能实现长效预防的治疗选择。”
舶望制药是一家处于临床阶段的生物技术公司,致力于开发新一代siRNA药物,舶望制药利用其行业领先的RADS(更强活性、持久性和安全性的RNA分子)平台技术,建立了丰富且差异化的siRNA候选药物管线,涵盖广泛的适应症。2025年与诺华达成多个项目合作,潜在总交易价值超过50亿美元。
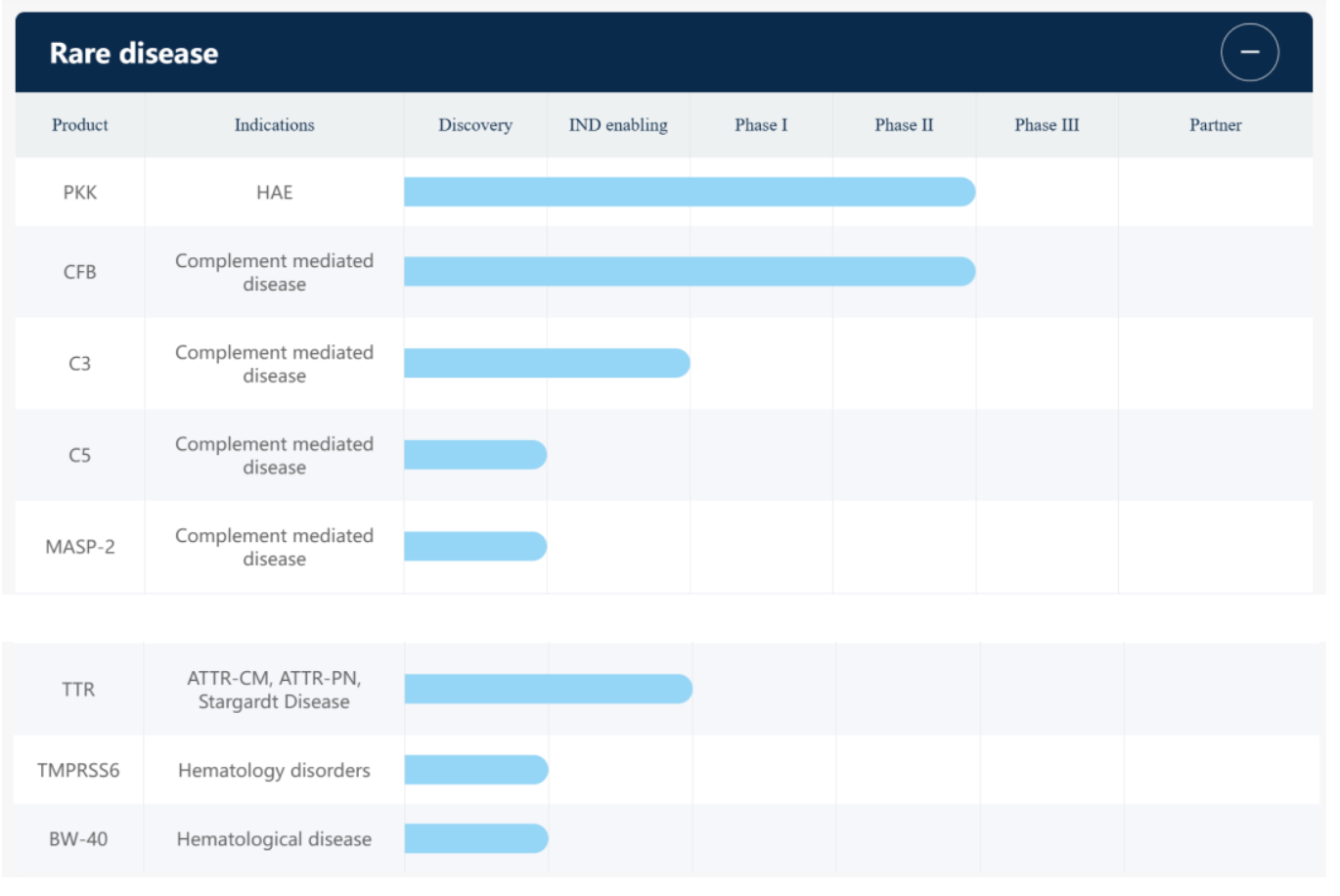
公司依托肝靶向与肝外递送技术平台,构建了覆盖心血管代谢、特殊疾病、病毒感染、中枢神经系统疾病及罕见病的多元化RNAi药物研发管线。目前,舶望制药已有七款RNAi候选药物进入临床研究。
|关于II期数据
2月26日,公司公布了最新2期临床数据,截至数据截止日,HAE发作率在600mg Q24W组下降100%,在300 mg Q24W组下降89%,在300mg Q12W组下降87%;期间80%(8/10)的患者保持无发作状态。
血浆PKK水平呈现快速且显著下降。在第85天,合并300mg剂量组(每24周给药组和每12周给药组)中,血浆PKK水平的平均降幅超过92%;600mg每24周给药组的降幅约达97%。
在完成169天随访的受试者中PKK的抑制作用持续维持:300mg每12周给药组在第169天的降幅达98%,600mg每24周给药组降幅达97%。
BW-20805总体安全性良好,主要为轻度、短暂的注射部位反应,未观察到严重不良事件。
上述结果展示了BW-20805稳健的药效学作用以及良好的安全性和耐受性,进一步支持其作为HAE长效预防性治疗药物的潜力。
参考资料:舶望制药