导语
α-1抗胰蛋白酶缺乏症 (alpha-1 antitrypsin deficiency, AATD) 是由14号染色体14q31-32.3区域编码α-1抗胰蛋白酶 (AAT) 的SERPINA1基因突变引起的一种常染色体共显性遗传性疾病,患者易发生慢性阻塞性肺病及肝脏损伤。据统计,AATD在北欧血统人群中相对常见,可累及1/1600~1/2000活产新生儿,但在东亚地区较为罕见,已纳入我国《第二批罕见病目录》。目前AATD肝病的发病机制尚不完全清楚,且针对AATD肝病患者,除肝移植外尚无大规模应用于临床的药物治疗,亟需开发新型的创新疗法。
近日,AIRNA公司宣布,其用于治疗治疗成年α-1抗胰蛋白酶缺乏症 ( AATD) 的在研RNA基因编辑疗法AIR-001在全球I期临床研究 (RepAIR1) 中成功完成首例患者给药并获得美国FDA授予的孤儿药资格认定 (ODD)。这一里程碑进展这标志着针对AATD底层病理机制的“源头治理”方案正式从实验室迈入临床验证阶段,有望彻底改变现有临床治疗中“治标不治本”的困境。
▲ 来源 iStock
告别永久性DNA改变:RNA编辑开辟基因治疗新纪元
当地时间2026年4月7日,AIRNA公司宣布,其用于治疗治疗成年α-1抗胰蛋白酶缺乏症 ( AATD) 的潜在同类最佳 (best-in-class) 在研RNA基因编辑疗法AIR-001在全球I期临床研究 (RepAIR1, NCT07431112) 中成功完成首例患者给药并获得美国FDA授予的孤儿药资格认定 (ODD)。这一里程碑进展这标志着针对AATD底层病理机制的“源头治理”方案正式从实验室迈入临床验证阶段,有望彻底改变现有临床治疗中“治标不治本”的困境。

▲ 新闻稿截图
AATD是一种由编码α-1抗胰蛋白酶 (AAT) 的SERPINA1基因突变 (主要为E342K点突变) 导致的常染色体共显性遗传性疾病。AAT是一种52kDa的糖蛋白,也是人血清中最丰富的蛋白酶抑制剂,主要由肝细胞合成并分泌到血液循环中,最终到达肺部。AATD的核心病理在于肝脏产生错误折叠的Z-AAT蛋白并在肝内蓄积,导致肝损伤,同时肺部缺乏功能性的M-AAT蛋白,从而面临进行性、不可逆的肺组织破坏风险。AATD的治疗主要采取支持性措施,以预防或减少慢性肝脏疾病并发症。对于进入终末期肝病的患者,肝移植是唯一有效的治疗手段。虽然目前已经有多款针对AATD肝病的细胞或基因治疗研发管线在积极推进,以抑制突变AAT的表达,促进AAT的分泌、降解或自噬(例如:突破,我国原创体内基因编辑疗法获批美国IND,进入扩展II/III期临床!;突破,又一款体内基因编辑疗法获FDA快速通道资格和孤儿药资格认定,临床加速!)。但也面临诸多挑战,例如需要每周用药的血浆提取AAT增补疗法 (如Prolastin-C等) 只能通过静脉注射提高血液中的AAT水平以保护肺部,但无法阻止突变蛋白在肝脏的产生和毒性积累。▲ AATD患者Z等位基因突变机制AATD的诊断需结合慢性肝病和慢性阻塞性肺病 (COPD) 的临床表现及相关辅助检查异常,血清 AAT水平、AAT表型及基因型来综合判断。AATD最常见的缺陷等位基因为Z (Glu342Lys) 和S (Glu264Val),其中Z等位基因可导致AAT蛋白错误折叠与聚合,约95%以上严重患者为PiZZ基因型。
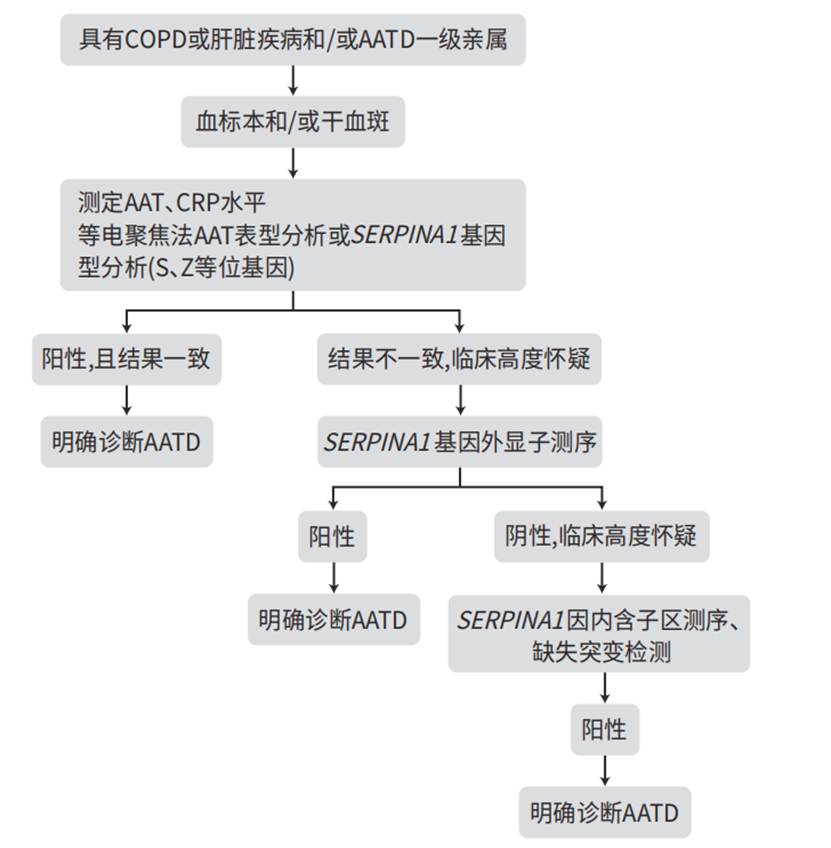
▲ AATD诊断流程
近年来,基因编辑技术的快速发展推动着医学领域迈入精准诊疗的新阶段,其中以CRISPR/Cas基因编辑为代表的DNA编辑技术已经在攻克诸多罕见性遗传病、肿瘤干预等领域展现了巨大潜力,但其可能引发的脱靶效应和不可逆的基因组改变,始终是临床应用与转化中需要面对的核心挑战。在此背景下,RNA编辑作为一种更为温和、安全的替代方案异军突起。RNA编辑是靶向转录后RNA序列的基因编辑技术,因其不会改变基因,也不会产生基因组的永久性变化的安全性和灵活性,成为当前基因编辑领域备受瞩目的研究热点。目前,已经有多个RNA编辑疗法进入临床试验阶段, 突显了该技术在基因治疗中的巨大潜力。

▲ RNA碱基编辑作用机制
AIR-001是一种通过皮下注射递送的化学修饰的GalNAc (N-乙酰半乳糖胺) 偶联寡核苷酸,当通过GalNAc受体介导内吞进入肝细胞后,AIR-001会特异性结合SERPINA1突变的mRNA形成局部的双链结构,进而招募内源性ADAR酶 (RNA特异性腺苷脱氨酶, Adenosine Deaminases Acting on RNA),将突变位点的腺苷 (A) 重新脱氨编辑回肌苷 (I),核糖体在读取mRNA密码子时再将肌苷 (I) 识别并解读为鸟苷 (G)。这不仅从翻译源头阻断了毒性Z-AAT蛋白的合成,解除了肝细胞的内质网应激;同时,修复后的mRNA能够顺利翻译出具有完整构象的野生型M-AAT蛋白,分泌入血后重塑肺部的蛋白酶/抗蛋白酶平衡。
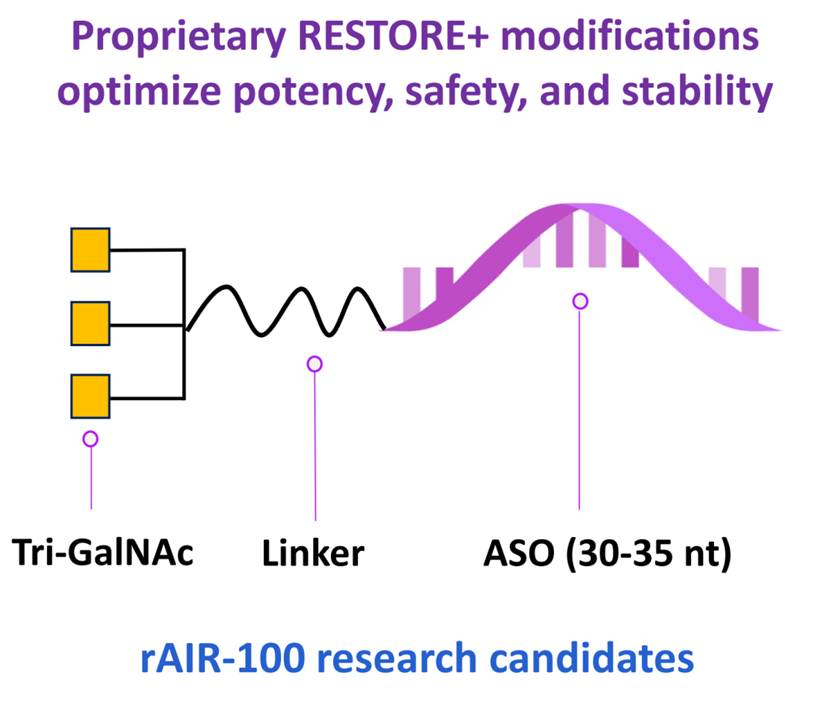 ▲ ARI-001设计原理
▲ ARI-001设计原理
与DNA水平的碱基编辑 (Base Editing) 或CRISPR切割DNA双链相比,AIR-001的RNA编辑是瞬时的、非永久性的,不需要引入外源性核酸酶,也不需要切割或永久性地改变患者的DNA,而是通过招募人体内源性的ADAR酶在RNA转录本水平上精准地进行单个碱基的修复。而且由于mRNA的半衰期很短,意味着如果患者一旦出现任何不良反应,只需要停药,患者体内的编辑作用就会迅速消失,不会对患者的基因组造成任何不可逆的“脱靶”切割,极大地降低了临床应用中的潜在风险。
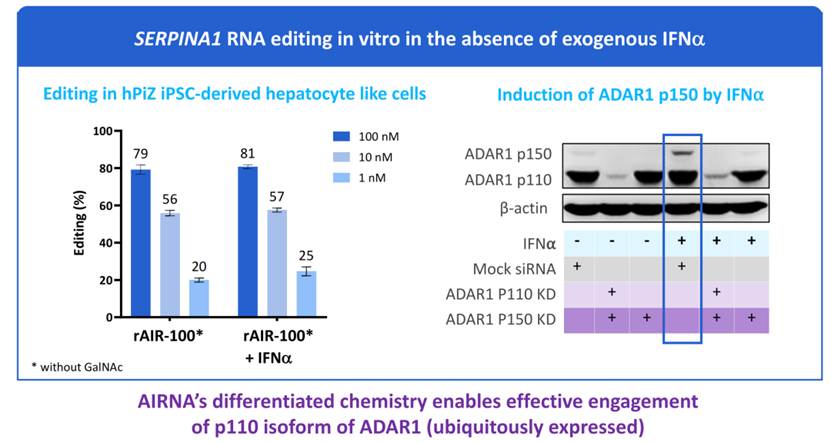
▲ ARI-001体外实验结果
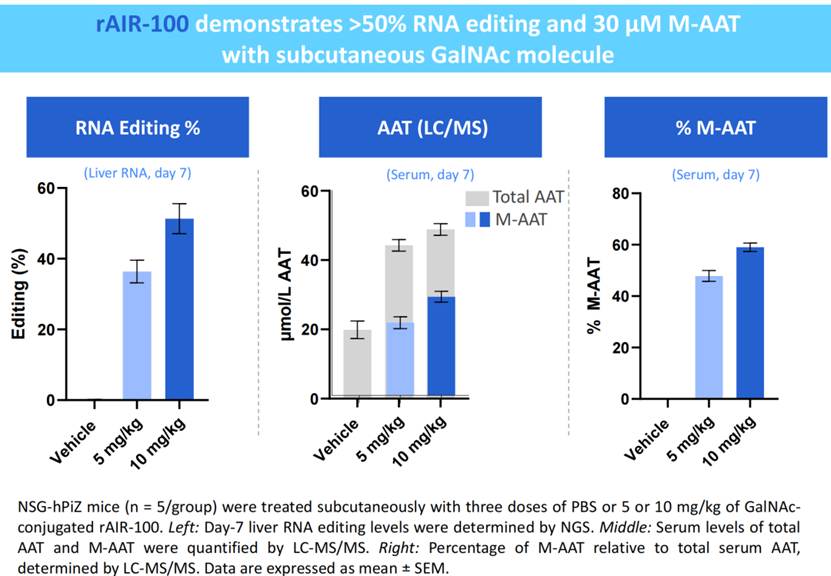
▲ ARI-001体内实验(小鼠)
结果在安全性方面,AIR-001在小鼠模型及非人类灵长类动物 (NHP) 模型中模型中均表现出极佳的耐受性。关键的肝脏损伤指标均未见具有临床意义的显著升高,也未观察到肝脏组织学上的严重炎症反应,而且未观察到明显的在非靶标基因上的脱靶编辑事件。
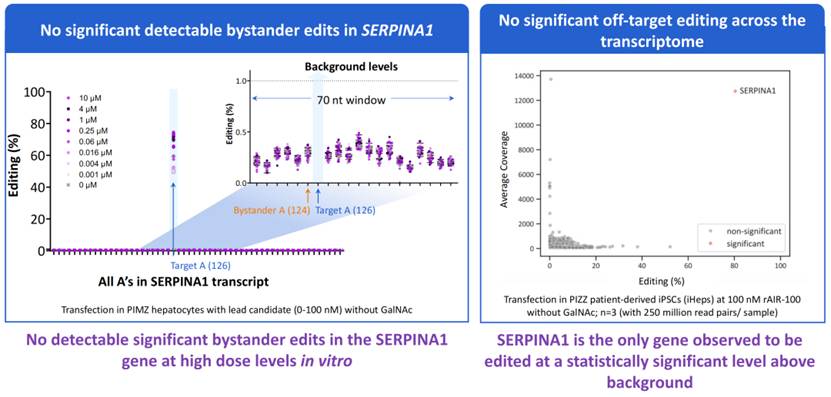
▲ ARI-001安全性结果
目前已在澳大利亚和英国启动招募的RepAIR1是一项多中心、开放标签的I期整合性单次递增及多次给药 (SAD/MAD) 临床研究,未来计划进一步扩展至全球11个国家的20个临床中心,预计入组54名携带PiZZ基因型的成年患者。该研究的核心临床终点不仅在于评估AIR-001的安全性与药代动力学 (PK) 特征,还在于追踪具有决定性意义的药效学 (PD) 生物标志物。与此同时,研究人员还将密切监测患者体内总AAT、功能性AAT、有害的Z-AAT以及有益的M-AAT水平的动态变化。
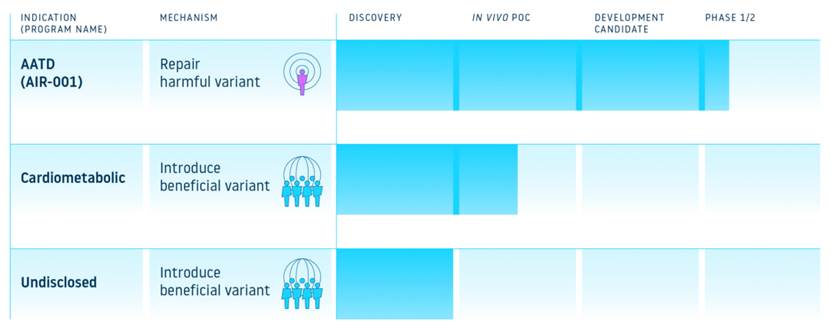
▲ AIRNA公司研发管线布局