4月14日,中国国家药品监督管理局(NMPA)最新药品通知件送达信息(官方拒绝/企业自行撤回)显示,齐鲁制药有限公司诺西那生钠注射液上市申请(受理号:CYHS2500029)在列。

![]()
药品审评中心(CDE)信息显示,齐鲁制药该NDA申请于2025年1月3日获受理(注册分类:仿制4类)。
Spinraza(Nusiersen/诺西那生钠)是经修饰的反义寡核苷酸(antisense oligonucleotide。ASO),通过与SMN2外显子7的剪切位点结合,降低被截断的机会,增加全长SMN蛋白的产生,从而治疗疾病。
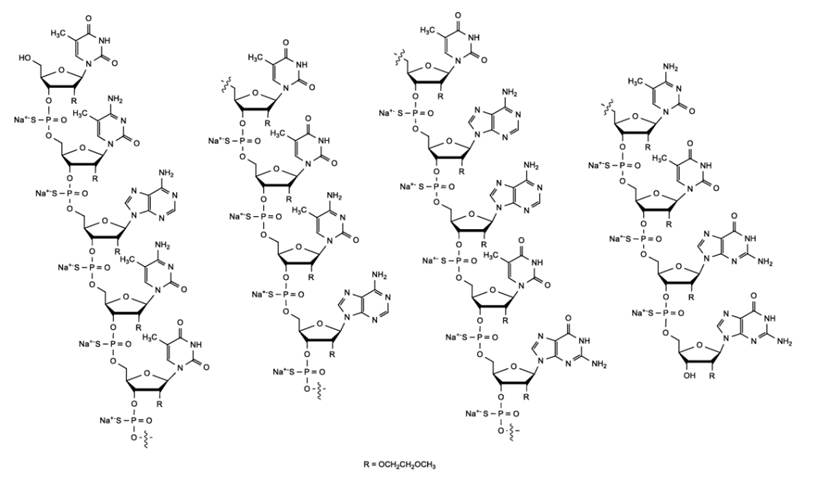
诺西那生钠最早由冷泉港实验室和Ionis Pharmaceuticals合作开发,2015年渤健获得全球开发、生产和商业化权利。
2016年12月,FDA批准上市,商品名:Spinraza,成为首个治疗儿童和成人SMA的药物。

2019年2月,NMPA以优先审评方式批准诺西那生钠注射液上市,用于治疗5q脊髓性肌萎缩症(SMA)。
诺西那生钠以治疗费用高昂闻名,美国上市后定价212万美元,合计1350万人民币。国内每针定价70万,每年需反复注射且属于完全自费药物,不过2022年被纳入国家医保名单,单针费用降至3万。
国内方面,除齐鲁制药外,重庆药友制药和成都国为生物本药的仿制药NDA分别于2024年9月和2025年3月获CDE受理(受理号:CYHS2402891、CYHS2501093)。不过重庆药友制药出现在2025年11月17日的药品通知件中。

![]()
扩展阅读:
1、2025年11月,FDA批准诺华(Novartis)鞘内注射Onasemnogene Abeparvovec(索伐瑞韦、Oav101 IT)上市,商品名:Itvisma,适应症:年龄≥2岁确认SMN1(运动神经元存活基因1)基因突变的脊髓性肌萎缩症(SMA)患者,不依赖体重给药!诺华脊髓性肌萎缩基因疗法再获批。2025年8月,CDE受理其上市申请(受理号JXSS2500106),上月优先审评!诺华脊髓性肌萎缩基因疗法国内上市获受理。
2、2025年5月,北京锦篮基因科技启动一项GC101腺相关病毒注射液鞘内(IT)注射治疗2型脊髓性肌萎缩症(SMA)患者关键性3期临床试验,国产脊髓性肌萎缩症基因疗法国内3期临床启动。3、2025年2月,罗氏Evrysdi(Risdiplam/利司扑兰)片获FDA批准用于治疗脊髓性肌萎缩(SMA),首个&唯一!罗氏脊髓性肌萎缩口服片剂获批。