2026年4月27日,Intellia Therapeutics宣布已正式向美国FDA滚动递交其在研CRISPR基因编辑疗法Lonvoguran Ziclumeran(lonvo-z)的生物制品许可申请(BLA),将其作为治疗遗传性血管性水肿(HAE)的一次性疗法,预计于2026年下半年完成申请,并有望在2027年上半年获批上市。
关于Lonvoguran Ziclumeran (lonvo-z)
Lonvoguran Ziclumeran(NTLA-2002)是一款基于CRISPR/Cas9技术开发的创新型基因治疗药物。它最大的特点在于,这是一款体内(in vivo)CRISPR基因编辑疗法,设计为在门诊环境下即可完成的一次性给药治疗。
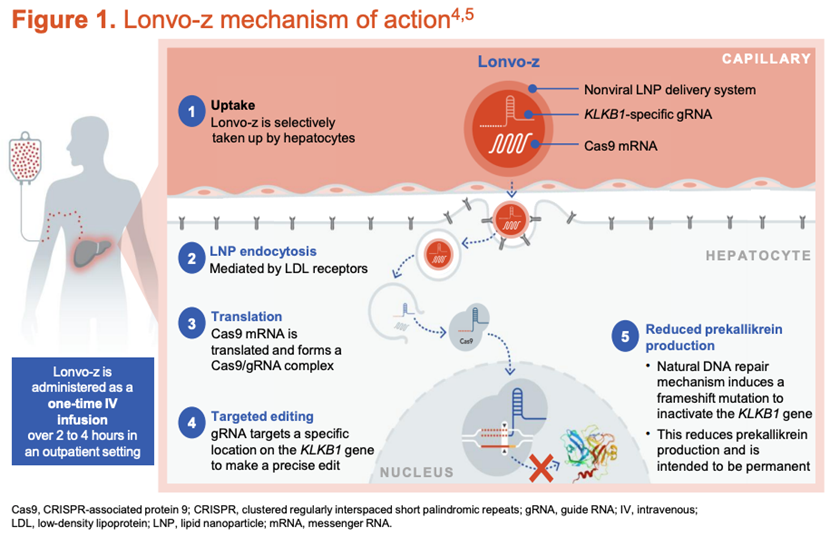
该药物的作用机制非常明确:它旨在通过单次注射,精准失活患者体内的激肽释放酶B1(KLKB1)基因。这一基因被“敲除”后,能够永久性地降低体内血浆激肽释放酶和缓激肽的水平,从而从根本上阻断导致严重水肿的病理通路。凭借其巨大的治疗潜力,lonvo-z此前已获得美国FDA授予的再生医学先进疗法(RMAT)认定和孤儿药资格,以及欧洲EMA的优先药物(PRIME)等五项国际重磅监管资格认定。
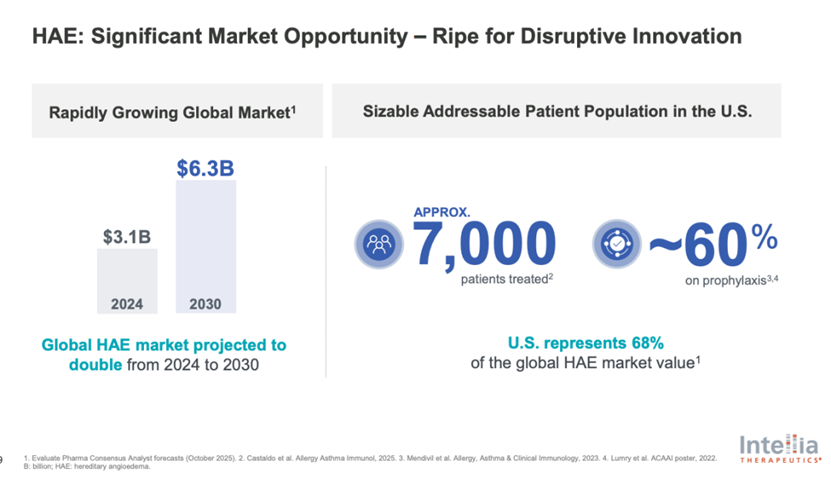
它针对的是怎样的疾病?遗传性血管性水肿(HAE)是一种罕见且可能危及生命的遗传性疾病,全球发病率约为五万分之一。HAE患者会经历严重、反复且不可预测的身体器官和组织的炎症性肿胀。目前的治疗标准通常需要患者终身用药,包括每周多达两次的静脉或皮下注射,或每天口服药物来控制发作。然而,即使在如此高频的长期给药下,部分患者的“突破性”水肿发作依然时有发生,身心和经济负担极其沉重。
HAELO试验:3期临床数据
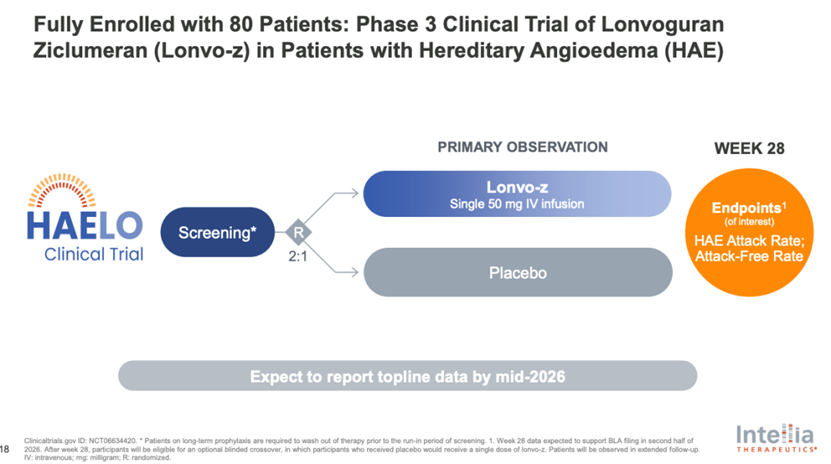
在宣布递交上市申请的同一天,Intellia还公布了lonvo-z在针对HAE的3期临床试验(HAELO)中的积极顶线数据。数据显示:该试验成功达到了主要终点以及所有关键次要终点。 在长达六个月的主要观察期内,绝大多数接受了单次lonvo-z治疗的患者不仅实现了HAE发作的“零发生”(freedom from attacks),并且完全摆脱了对日常预防性治疗药物的依赖。这一惊艳的数据证实了:只需打一针,患者就有极大可能彻底摆脱长期的痛苦与终身用药的枷锁。
里程碑意义
首先,这是全球首款走向商业化的“体内”CRISPR基因编辑疗法。 虽然医学界此前已有CRISPR疗法获批,但那属于“体外(ex vivo)”编辑,需要将患者的干细胞提取出体外、在实验室进行编辑后再回输,整个过程需要清髓性化疗、长期住院,且依赖高度专业的移植中心,风险高且门槛极高。而lonvo-z开启了“体内治疗”的新纪元——基因编辑工具就像普通生物药一样,通过门诊点滴直接注射入患者体内完成靶向编辑。这一跨越极大地简化了治疗流程,拓宽了基因编辑技术的应用场景与可及性。
其次,它代表了罕见病治疗从“终身慢性管理”向“一次性治愈”的范式转变。正如Intellia总裁兼首席执行官John Leonard博士所言,lonvo-z的临床结果坚定了人们对其彻底改变HAE治疗格局的信心。只需一次给药,就能让患者免除终身的预防性治疗和频繁发作的恐惧。这是对“治标不治本”的传统医学模式的一次颠覆,为数以万计的患者家庭带来了回归正常生活的曙光。
最后,加速了前沿生物技术向临床转化的监管路径。依托FDA的RMAT认定,Intellia获准采用“滚动递交”机制,允许企业分批次提交申请材料,从而极大加快了FDA的审评速度。同时,Intellia还参与了FDA的化学、制造和控制(CMC)开发与准备试点项目。这些监管端的一系列“绿色通道”,不仅为lonvo-z在2027年上半年的顺利商业化铺平了道路,也证明了监管机构对具有颠覆性潜力的体内基因编辑技术的支持与认可,为未来更多基因疗法的研发树立了标杆。