2026年4月15日,澳大利亚临床阶段免疫治疗公司Immutep Limited(NASDAQ: IMMP;ASX: IMM)宣布,其核心在研药物eftilagimod alfa(efti)获美国FDA授予软组织肉瘤(STS)适应症的孤儿药认定(Orphan Drug Designation, ODD)。

受此消息刺激,公司股价当日收盘暴涨73%至0.54美元,创阶段性新高。
此次孤儿药认定距Immutep宣布终止TACTI-004 III期非小细胞肺癌研究不到一个月。该研究因独立数据监察委员会建议无效而提前停止。
疗效数据超越预设目标近50%
该孤儿药认定基于研究者发起的II期EFTISARC-NEO临床试验的积极数据。该研究评估efti联合放疗及默沙东Keytruda(帕博利珠单抗)用于可切除软组织肉瘤新辅助治疗的疗效与安全性。
在38例可评估患者中,研究达到主要终点,中位肿瘤玻璃样变/纤维化率达51.5%,显著超越预设的35%目标阈值,较单纯放疗的历史基准(约15%)提升逾3倍,具有高度统计学显著性(p<0.001)。
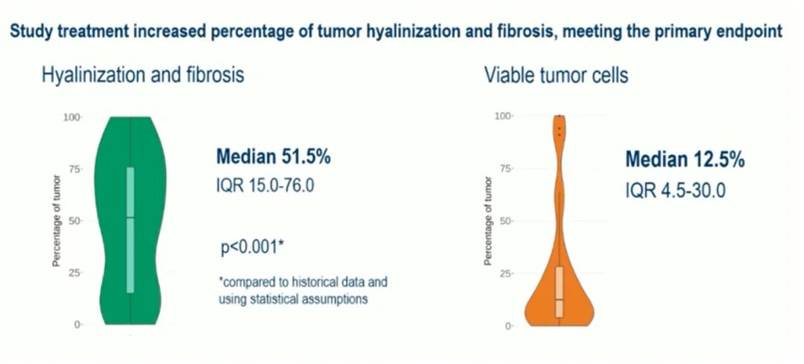
肿瘤玻璃样变/纤维化是软组织肉瘤手术切除时的早期替代终点,与患者无病生存期及总生存期改善密切相关。
值得注意的是,该疗效在包括黏液纤维肉瘤(N=16)、未分化多形性肉瘤(N=10)及恶性外周神经鞘瘤(N=2)在内的10种不同肉瘤亚型中均有体现,其中不乏预后极差的罕见高度侵袭性肿瘤。
转化医学数据佐证免疫激活机制
2025年11月在CTOS年会公布的转化医学数据显示,efti的抗原呈递细胞激活机制在软组织肉瘤中同样适用。
前20例接受手术患者的生物标志物分析表明,外周血中CXCL9(2.5倍,p<0.01)、CXCL10(1.8倍,p<0.0001)、IL-23(2.2倍,p<0.05)及IFN-γ(2.5倍,p<0.05)等关键细胞因子/趋化因子水平显著上调,且IFN-γ升高与病理缓解呈正相关。

FDA孤儿药认定为Immutep带来多重监管与商业优势,包括研发税收抵免、申请费用豁免及获批后7年美国市场独占权等。
高管同步增持
同日提交的Form 3文件显示,公司高管层持股情况如下:首席运营官Deanne Diem Miller初始持股2,867,305股,首席执行官兼首席财务官Marc Voigt持股14,792,145股。根据Simply Wall St数据,Miller近期增持24.3%,Voigt持股规模位列公司主要股东前列。
结束语
efti在软组织肉瘤领域的突破为公司开辟了新的价值验证路径,尤其是在该适应症尚缺乏有效新辅助治疗方案的背景下。随着EFTISARC-NEO研究的生存数据逐步成熟,软组织肉瘤有望成为efti首个进入注册性III期开发的适应症领域。